üĒį┤Ż║ŠW(w©Żng)Įj(lu©░)┘Yį┤ 2022-12-10 20:24:44
╦ßēA¹}╩Ū╗»īW(xu©”)ūŅ║¾ę╗▓┐Ęųā╚(n©©i)╚▌Ż¼ę▓╩Ūųą┐╝Ą─ųžųąų«ųžŻ¼Ė„┤¾ĘĮ│╠╩ĮĖ³╩Ū┐╝ŠĒĄ─│Ż┐═ĪŻ▀@└’įö╝Ü(x©¼)Ąž┐éĮY(ji©”)┴╦▀@ę╗īŻŅ}Ą─ųž³c(di©Żn)ų¬ūRŻ¼╚ń╣¹─Ń▀Ćėą╚╬║╬ę╔å¢Ą─įÆŻ¼ę╗Č©ę¬ūą╝Ü(x©¼)ķåūxĪŻ
ę╗Īó╦ß╝░╦ߥ─═©ąį
╦ߥ─Č©┴xŻ¼ļŖļxĢr(sh©¬)╔·│╔Ą─Ļ¢ļxūė╚½▓┐Č╝╩ŪH+ĪŻ╦ß╩Ūė╔Üõļxūė║═╦ßĖ∙ļxūėśŗ(g©░u)│╔ĪŻ
1.ØŌ¹}╦ßĪóØŌ┴“╦ߥ─╬’└Ēąį┘|(zh©¼)Īó╠žąįĪóė├═Š
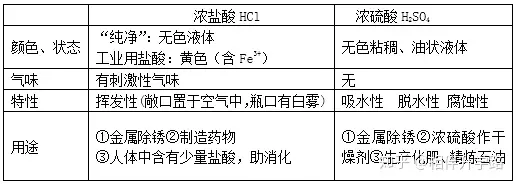
2.╦ߥ─═©ąįŻ║¹} ╦ß HCl ┴“ ╦ß H2SO4
╦ß╩╣ūŽ╔½╩»╚’įćę║ūā╝tŻ¼╩╣¤o╔½Ęė╠¬įćę║▓╗ūā╔½ĪŻ
Įī┘+╦ß→¹}+ÜõÜŌ
Zn+2HCl=ZnCl2+H2↑
Zn+ H2SO4 =ZnSO4+H2↑
ēAąįč§╗»╬’+╦ß→¹}+╦«
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
ēA+╦ß→¹}+╦«
NaOH+HCl=NaCl+ H2O
Cu(OH)2+H2SO4= CuSO4+2H2O
¹}+╦ß→┴Ēę╗ĘN¹}+┴Ēę╗ĘN╦ß
AgNO3+HCl=AgCl↓+HNO3
BaCl2+H2SO4=BaSO4↓ +2HCl
ūóęŌŻ║(1)į┌‘Įī┘+╦ß→¹}+ÜõÜŌ’ųąŻ¼╦ß═©│ŻųĖĄ─╩ŪŽĪ┴“╦ß║═ŽĪ¹}╦߯¼▓╗─▄╩ŪØŌ┴“╦ß╗“Ž§╦ßĪŻ
ę“?y©żn)ķØŌ┴“╦ß╗“Ž§╦ßČ╝ėąÅ?qi©óng)č§╗»ąįŻ¼┼cĮī┘Ę┤æ¬(y©®ng)Ģr(sh©¬)▓╗─▄╔·│╔ÜõÜŌČ°╔·│╔┴╦╦«ĪŻ
(2)═©▀^Įī┘Ė·╦ߥ─Ę┤æ¬(y©®ng)Ūķørī¦(d©Żo)│÷Įī┘╗ŅäėĒśą“▒ĒŻ║
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
Įī┘╗Ņäėąįė╔ÅŖ(qi©óng)ųØu£p╚§Įī┘╗ŅäėąįĒśą“ųąŻ¼Įī┘╬╗ų├įĮ┐┐Ū░Ż¼╗ŅäėąįįĮÅŖ(qi©óng)Ż¼Ę┤æ¬(y©®ng)įĮäĪ┴ęŻ¼╦∙ąĶĢr(sh©¬)ķgįĮČ╠ĪŻ
(3)ØŌ┴“╦ߊ▀ėą╬³╦«ąįŻ¼═©│Żė├╦³ū„×ķĖ╔į’ä®ĪŻ
┴“╦ß▀ĆŠ▀ėą├ō╦«ąįŻ¼╦³ī”Ųż─w╗“ę┬Ę■ėą║▄ÅŖ(qi©óng)Ą─Ė»╬gąįĪŻ
ŽĪßīØŌ┴“╦ßĢr(sh©¬)ę╗Č©ę¬░čØŌ┴“╦ßčžų°Ų„▒┌┬²┬²Ąžūó╚ļ╦«└’Ż¼▓ó▓╗öÓöćäėŻ¼Ūą▓╗┐╔░č╦«Ą╣▀M(j©¼n)ØŌ┴“╦ß└’Ż¼╚ń╣¹░č╦«ūó╚ļØŌ┴“╦ß└’Ż¼╦«Ą─├▄Č╚▌^ąĪŻ¼Ģ■ĖĪį┌┴“╦ß╔Ž├µŻ¼╚▄ĮŌĢr(sh©¬)Ę┼│÷Ą─¤ßĢ■╩╣╦«┴ó┐╠Ęą“vŻ¼╩╣┴“╦ßę║Ž“╦─╠Ä’w×RŻ¼╚▌ęū░l(f©Ī)╔·╩┬╣╩ĪŻ
Č■ĪóēA╝░ēAĄ─═©ąį
Č©┴xŻ║ļŖļxĢr(sh©¬)╔·│╔Ą─ĻÄļxūė╚½▓┐╩ŪOH-ļxūėĪŻēA╩Ūė╔Įī┘ļxūė(╗“õ@Ė∙ļxūė)║═Üõč§Ė∙ļxūėśŗ(g©░u)│╔ĪŻ
1.Üõč§╗»ŌcĪóÜõč§╗»Ō}Ą─╬’└Ēąį┘|(zh©¼)Īóė├═Š
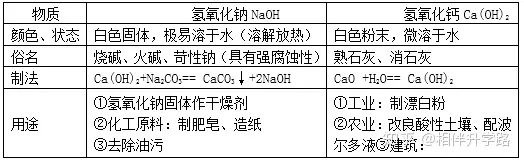
2.ēAĄ─═©ąį
ēA╩╣ūŽ╔½╩»╚’įćę║ūā╦{(l©ón)Ż¼╩╣¤o╔½Ęė╠¬įćę║ūā╝tĪŻ
Üõč§╗»Ōc╩╣ūŽ╔½╩»╚’įćę║ūā╦{(l©ón)Ż¼¤o╔½Ęė╠¬įćę║ūā╝tĪŻ
Üõč§╗»Ō}╩╣ūŽ╔½╩»╚’įćę║ūā╦{(l©ón)Ż¼¤o╔½Ęė╠¬įćę║ūā╝tĪŻ
╦ßąįč§╗»╬’+ēA→¹}+╦«
2NaOH+CO2=Na2CO3+H2O Ca(OH)2+CO2=CaCO3↓+H2O
╦ß+ēA→¹}+╦«
NaOH+HCl=NaCl+H2O
Ca(OH)2+H2SO4= CaSO4+2H2O
¹}+ēA→┴Ēę╗ĘN¹}+┴Ēę╗ĘNēA
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
ūóęŌŻ║(1)ų╗ėą┐╔╚▄ąįēA▓┼─▄Ė·ę╗ą®ĘŪĮī┘č§╗»╬’░l(f©Ī)╔·Ę┤æ¬(y©®ng)Ż¼▀@ą®ĘŪĮī┘č§╗»╬’╩Ū╦ßąįč§╗»╬’ĪŻ╦ßąįč§╗»╬’ČÓöĄ(sh©┤)─▄╚▄ė┌╦«Ż¼Ė·╦«╗»║Ž╔·│╔╦ßĪŻ
(2)¹}║═ēAĘ┤æ¬(y©®ng)Ģr(sh©¬)Ż¼▒žĒÜā╔š▀Č╝╩Ū┐╔╚▄Ą─Ż¼Ūę╔·│╔╬’ų«ę╗╩Ū│┴ĄĒŻ¼Ę┤æ¬(y©®ng)▓┼─▄▀M(j©¼n)ąąĪŻ
(3)Ģ°īæēAĖ·─│ą®Įī┘č§╗»╬’Ę┤æ¬(y©®ng)Ą─╗»īW(xu©”)ĘĮ│╠╩Į
ĻP(gu©Īn)ė┌▀@ŅÉĘ┤æ¬(y©®ng)╗»īW(xu©”)ĘĮ│╠╩ĮĄ─Ģ°īæėą═¼īW(xu©”)ĖąĄĮ║▄└¦ļyŻ¼×ķ┤╦Ż¼┐╔Ž╚īæ│÷ĘŪĮī┘č§╗»╬’Ė·╦«Ę┤æ¬(y©®ng)Ż¼╔·│╔║¼č§╦ߥ─╗»īW(xu©”)ĘĮ│╠╩ĮŻ¼į┘ęį║¼č§╦ß║═ēAŽÓ╗źĮ╗ōQ│╔Ęųīæ│÷╔·│╔╬’ĪŻā╔╩Į║Ž▓ó│╔ę╗éĆ(g©©)╗»īW(xu©”)ĘĮ│╠╩ĮĪŻ
╚²Īó│ŻęŖĄ─¹}╝░¹}Ą─ąį┘|(zh©¼)
1.│ŻęŖĄ─¹}
Č©┴xŻ║─▄ĮŌļx│÷Įī┘ļxūė(╗“NH4+)║═╦ßĖ∙ļxūėĄ─╗»║Ž╬’ĪŻ
ūóŻ║┤╦Ģr(sh©¬)Ą─¹}▓╗╩ŪųĖ╩│¹}Ż¼╩│¹}Ą─ų„ę¬│╔Ęų╩ŪNaClĪŻ
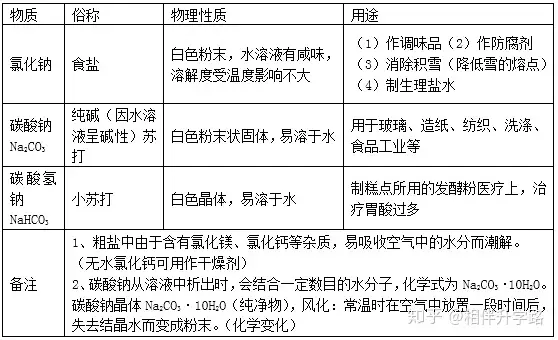
2.Š½¹}╠ß╝ā
╚ź│²▓╗╚▄ąįļs┘|(zh©¼)Ż¼Ą├ĄĮĄ─Š½¹}ųą▀Ć║¼ėą┬╚╗»µVĪó┬╚╗»Ō}Ą╚┐╔╚▄ąįļs┘|(zh©¼)ĪŻ
(1)īŹ(sh©¬)“×(y©żn)▓Į¾EŻ║╚▄ĮŌĪó▀^×VĪóš¶░l(f©Ī)

(2)īŹ(sh©¬)“×(y©żn)āxŲ„
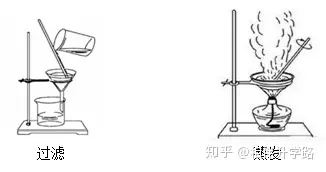
ūóęŌŻ║
ó┘ š¶░l(f©Ī)├¾╩Ū┐╔ęįų▒Įė╝ė¤ßĄ─āxŲ„Ż¼ę║¾w¾wĘe▓╗─▄│¼▀^š¶░l(f©Ī)├¾2/3.
ó┌ ╚▄ĮŌĢr(sh©¬)ė├▓Ż┴¦░¶öć░ĶŻ¼─┐Ą─╩Ū╝ė┐ņ╚▄ĮŌĪŻ
ó█ ╝ė¤ßĢr(sh©¬)ė├▓Ż┴¦░¶öć░ĶŻ¼Ę└ų╣Šų▓┐£žČ╚▀^Ė▀įņ│╔ę║Ą╬’w×R
ó▄ ┤²š¶░l(f©Ī)├¾ųą│÷¼F(xi©żn)▌^ČÓ╣╠¾wĢr(sh©¬)═Żų╣╝ė¤ßŻ¼└¹ė├ėÓ¤ß╩╣×Vę║š¶Ė╔Ż¼▓╗─▄īó×Vę║═Ļ╚½š¶Ė╔▓┼═Żī”ė┌ų╣╝ė¤ßĪŻ
3.¹}Ą─╗»īW(xu©”)ąį┘|(zh©¼)
¹}╚▄ę║+Įī┘→¹}©@+Įī┘©@
CuSO4+Zn= ZnSO4+Cu
¹}+╦ß→¹}©@+ ╦ß©@
BaCl2+H2SO4=BaSO4↓ +2HCl
¹}╚▄ę║+ēA╚▄ę║→¹}©@+ēA©@
3NaOH+FeCl3=3NaCl+Fe(OH)3 ↓
¹}╚▄ę║+¹}╚▄ę║→¹}©@+¹}©@
AgNO3+NaCl=AgCl↓+NaNO3
ūóęŌŻ║į┌Įī┘╗ŅäėĒśą“▒ĒųąŻ¼ų╗ėą┼┼į┌Ū░├µĄ─Įī┘▓┼─▄░č┼┼į┌║¾├µĄ─Įī┘Å─╦³éāĄ─¹}╚▄ę║ųąų├ōQ│÷üĒĪŻĄ½KĪóCaĪóNa╚²ĘNĮī┘┼c¹}╚▄ę║Ą─Ę┤æ¬(y©®ng)╠ž╩ŌŻ¼▀@└’▓╗ę¬Ū¾ĪŻ
╦─ĪóÅ═(f©┤)ĘųĮŌĘ┤æ¬(y©®ng)║═╦ßēA¹}Ę┤æ¬(y©®ng)
1.Å═(f©┤)ĘųĮŌĘ┤æ¬(y©®ng)
Å═(f©┤)ĘųĮŌĘ┤æ¬(y©®ng)Ą─Č©┴x╩ŪŻ║ė╔ā╔ĘN╗»║Ž╬’ŽÓ╗źĮ╗ōQ│╔ĘųŻ¼╔·│╔┴Ē═Ōā╔ĘN╗»║Ž╬’Ą─Ę┤æ¬(y©®ng)ĪŻ
═©╩ĮŻ║AB+CD=AD+CB
2.░l(f©Ī)╔·Ą─Śl╝■
ā╔ĘN╬’┘|(zh©¼)į┌╚▄ę║ųąŽÓ╗źĮ╗ōQļxūėŻ¼╔·│╔╬’ųą╚ń╣¹ėą│┴ĄĒ╬÷│÷ĪóÜŌ¾wĘ┼│÷╗“ėą╦«╔·│╔Ż¼Å═(f©┤)ĘųĮŌĘ┤æ¬(y©®ng)Š∙┐╔ęį░l(f©Ī)╔·ĪŻ
3.ēA┼c╦ßąįč§╗»╬’Ę┤æ¬(y©®ng)▓╗ī┘ė┌Å═(f©┤)ĘųĮŌĘ┤æ¬(y©®ng)
╬ÕĪó╩ņėø╦ßĪóēAĪó¹}Ą─╚▄ĮŌąį
╦ßĪóēAĪó¹}Ą─╚▄ĮŌąįėøæø┐┌įEŻ║
ēAųą░▒ĪóŌøĪóŌcĪóõ^ĪóŌ}┐╔╚▄
ŌøŌcõ@¹}Ž§╦ß¹}Ż¼ ╚½▓┐Č╝ī┘┐╔╚▄¹}ĪŻ
┴“╦ß¹}▓╗╚▄õ^║═ŃU;
┬╚╗»╬’▓╗╚▄Ńyüå╣»Ż¼ ╠╝╦ß¹}│²ŌøŌcõ@╚▄Ż¼Ųõ╦³▓╗╚▄ĪŻ
┴∙ĪóÄūéĆ(g©©)│ŻęŖļxūėĄ─Öz“×(y©żn)
1.Cl-ļxūėĄ─Öz“×(y©żn)
(Ęųäe×ķīŹ(sh©¬)“×(y©żn)▓┘ū„ īŹ(sh©¬)“×(y©żn)¼F(xi©żn)Ž¾ īŹ(sh©¬)“×(y©żn)ĮY(ji©”)šō ╗»īW(xu©”)ĘĮ│╠╩Į)
╚Ī╔┘┴┐śėŲĘė┌įć╣▄ųąŻ¼Ą╬╝ėAgNO3╚▄ę║║═ŽĪHNO3
ėą▓╗╚▄ė┌ŽĪŽ§╦ߥ─░ū╔½│┴ĄĒ╔·│╔
śėŲĘ║¼ėąCl-
AgNO3+KCl=AgCl↓+KNO3
2.SO42-ļxūėĄ─Öz“×(y©żn)
╚Ī╔┘┴┐śėŲĘė┌įć╣▄ųąŻ¼Ą╬╝ėBa(NO3)2╚▄ę║║═ŽĪHNO3
ėą▓╗╚▄ė┌ŽĪŽ§╦ߥ─░ū╔½│┴ĄĒ╔·│╔
śėŲĘ║¼ėąSO42-
Ba(NO3)2+H2SO4=BaSO4↓+2HNO3
3. CO32-ļxūėĄ─Öz“×(y©żn)
╚Ī╔┘┴┐śėŲĘė┌įć╣▄ųąŻ¼Ą╬╝ėŽĪHCl,īó╔·│╔Ą─ÜŌ¾w═©╚ļ│╬ŪÕ╩»╗ę╦«
ėą¤o╔½ÜŌ¾w╔·│╔Ż¼įōÜŌ¾w╩╣│╬ŪÕ╩»╗ę╦«ūā£åØß
śėŲĘ║¼ėąCO32-
K2CO3+2HCl=2KCl+ CO2↑+H2O
CO2+Ca(OH)2= CaCO3↓+ H2O
4.Öz“×(y©żn)NH4+
╚Ī╔┘┴┐┤²Öz╬’ė┌ØŹā¶Ą─įć╣▄ųąŻ¼Ą╬╚ļ▀m┴┐NaOH╚▄ę║▓ó╝ė¤ßŻ¼ėą╩╣?ji©”)±Ą─╝t╔½╩»╚’įć╝łūā│╔╦{(l©ón)╔½Ą─ÜŌ¾w«a(ch©Żn)╔·ĪŻ
5.ĶbäeŽĪ¹}╦ß║═ŽĪ┴“╦ß
Ęųäe╚Ī╔┘┴┐┤²Özę║¾wė┌ā╔ų¦ØŹā¶Ą─įć╣▄ųąŻ¼Ė„Ą╬╚ļÄūĄ╬BaCl2╚▄ę║Ż¼ėą░ū╔½│┴ĄĒ«a(ch©Żn)╔·Ą─įŁ╚▄ę║╩ŪŽĪ┴“╦߯¼¤o¼F(xi©żn)Ž¾«a(ch©Żn)╔·Ą─įŁ╚▄ę║╩ŪŽĪ¹}╦ßĪŻ
Ų▀Īó│ŻęŖį¬╦ž║═įŁūėłF(tu©ón)Ą─╗»║Žār(ji©ż)
(š²ār(ji©ż))ę╗ÜõŌøŌcŃyŻ¼Č■Ō}µVõ^õ\Ż¼╚²õXĪó╦─╣ĶĪó╬ÕĄ¬┴ūĪŻ
(žō(f©┤)ār(ji©ż))žō(f©┤)ę╗ār(ji©ż)Ż║Ę·Īó┬╚ĪóõÕĪóĄŌ;
žō(f©┤)Č■ār(ji©ż)Ż║č§║═┴“ĪŻ
(┐╔ūāš²ār(ji©ż))Ż║ę╗Č■Ń~╣»Ż¼Č■╚²ĶFŻ¼Č■╦─╠╝Ż¼╦─┴∙┴“ĪŻ
įŁūėłF(tu©ón)Ą─╗»║Žār(ji©ż)Ż║
žō(f©┤)ę╗ār(ji©ż)Ż║Üõč§Ė∙(OH)Ż¼Ž§╦ßĖ∙(NO3)Ż¼┬╚╦ßĖ∙(ClO3)Ż¼Ė▀Õi╦ßĖ∙(MnO4);
žō(f©┤)Č■ār(ji©ż)Ż║┴“╦ßĖ∙(SO4)Ż¼╠╝╦ßĖ∙(CO3)Ż¼üå┴“╦ßĖ∙(SO3)Ż¼Õi╦ßĖ∙(MnO4);
žō(f©┤)╚²ār(ji©ż)Ż║┴ū╦ßĖ∙(PO4); š²ę╗ār(ji©ż)Ż║õ@Ė∙(NH4)ĪŻ
░╦Īó╩ņėø╦ūĘQĪóų„ę¬│╔Ęų║═╗»īW(xu©”)╩Į
╔·╩»╗ę—— CaO
╩ņ╩»╗ę——Ca(OH)2
╩»╗ę╩»Īó┤¾└Ē╩»—— CaCO3
╩│¹}——NaCl
╗ēAĪó¤²ēAĪó┐┴ąįŌc—— NaOH
╝āēAĪó╠K┤“——Na2CO3
ąĪ╠K┤“—— NaHCO3
ĶFõPĪó│ÓĶFĄV——Fe2O3
│ÓĶFĄV—— Fe3O4
Įäé╩»Īó╩»─½—— C
Ė╔▒∙——CO2
▒∙—— H2O
╠ņ╚╗ÜŌ(╝ū═ķ)——CH4
ŠŲŠ½(ęę┤╝)—— C2H5OH
┤ū╦ß(ęę╦ß)——CH3COOH
Š┼Īó│ŻęŖ╬’┘|(zh©¼)Ą─Ņü╔½
╝t╔½Ą─╣╠¾w——CuĪóFe2O3 ĪóP(╝t┴ū)
║┌╔½Ą─╣╠¾w——CĪóCuOĪóFe3O4ĪóFeOĪóMnO2
░ū╔½Ą─╣╠¾w——KClO3ĪóP2O5ĪóP(░ū┴ū)ĪóCuSO4(¤o╦«┴“╦ßŃ~)ĪóKClĪóNaClĄ╚
░ĄūŽ╔½Ą─╣╠¾w——KMnO4
³S╔½Ą─╣╠¾w—— S
╦{(l©ón)╔½Ą─╣╠¾w——CuSO4•5H2O
╦{(l©ón)╔½│┴ĄĒ——Cu(OH)2
╝t║ų╔½│┴ĄĒ——Fe(OH)3
│ŻęŖ▓╗╚▄ė┌╦ߥ─░ū╔½│┴ĄĒ——BaSO4ĪóAgCl
╚▄ė┌╦ß▓óĘ┼│÷╩╣│╬ŪÕ╩»╗ę╦«ūā£åØߥ─ÜŌ¾wĄ─░ū╔½│┴ĄĒ——BaCO3ĪóCaCO3
╚▄ė┌╦ߥ½▓╗«a(ch©Żn)╔·ÜŌ¾wĄ─░ū╔½│┴ĄĒ——Mg(OH)2ĪóAl(OH)3Ą╚▓╗╚▄ąįēAĄ─│┴ĄĒ
╦{(l©ón)╔½Ą─╚▄ę║—— CuSO4ĪóCuCl2ĪóCu(NO3)2Ą╚║¼Cu2+╚▄ę║
£\ŠG╔½Ą─╚▄ę║——FeSO4ĪóFeCl2Ą╚║¼F(xi©żn)e2+╚▄ę║
³S╔½Ą─╚▄ę║——FeCl3ĪóFe2(SO4)3ĪóFe(NO3)3Ą╚║¼F(xi©żn)e3+╚▄ę║
ča(b©│)│õŽ┬┴ąĘ┤æ¬(y©®ng)ĘĮ│╠╩ĮŻ║
1.Üõč§╗»Ń~Ė·ŽĪ¹}╦ßĘ┤æ¬(y©®ng)Ż║ Cu(OH)2 + 2HCl = CuCl2 + 2H2O ╦{(l©ón)╔½│┴ĄĒŽ¹╩¦
2.Üõč§╗»Ń~Ė·ŽĪ┴“╦ßĘ┤æ¬(y©®ng)Ż║ Cu(OH)2 + H2SO4 = CuSO4 + 2H2O ūā│╔╦{(l©ón)╔½╚▄ę║
3.Üõč§╗»ŌcĖ·┴“╦ßŃ~╚▄ę║Ę┤æ¬(y©®ng)Ż║2NaOH + CuSO4 = Na2SO4 + Cu(OH)2 ↓ ėą╦{(l©ón)╔½│┴ĄĒ«a(ch©Żn)╔·
4.Üõč§╗»ŌcĖ·┬╚╗»ĶF╚▄ę║Ę┤æ¬(y©®ng)Ż║3NaOH + FeCl3 = Fe(OH)3↓ +3NaCl ėą╝t║ų╔½│┴ĄĒ«a(ch©Żn)╔·
┼ąöÓ╚▄ę║Ą─╦ßēAąį
ė├ųĖ╩Šä®Ż¼╚▄ę║Ą─╦ßēAČ╚——ė├pHüĒ▒Ē╩ŠĪŻ
Ė╔į’䮥─▀xō±
1.ØŌ┴“╦ß┐╔Ė╔į’Ż║
╦ßąįÜŌ¾w(╚ńŻ║CO2ĪóSO2ĪóSO3ĪóNO2ĪóHClĪó)
ųąąįÜŌ¾w(╚ńŻ║H2ĪóO2ĪóN2ĪóCO)
Ī∙▓╗─▄Ė╔į’ēAąįÜŌ¾w(╚ńŻ║NH3)
2.Üõč§╗»Ōc╣╠¾wĪó╔·╩»╗ęĪóēA╩»╗ę┐╔Ė╔į’Ż║
ēAąįÜŌ¾w(╚ńŻ║NH3)
ųąąįÜŌ¾w(╚ńŻ║H2ĪóO2ĪóN2ĪóCO)
Ī∙▓╗─▄Ė╔į’╦ßąįÜŌ¾w(╚ńŻ║CO2ĪóSO2ĪóSO3ĪóNO2ĪóHCl)
3.¤o╦«┴“╦ßŃ~╣╠¾wė÷╦«ė╔░ū╔½ūā╦{(l©ón)╔½Ż¼┐╔Öz“×(y©żn)╦«Ą─┤µį┌Ż¼▓ó╬³╩š╦«š¶ÜŌĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖC(j©®)ĪóŲĮ░ÕĄ╚ęŲäėįO(sh©©)éõįLå¢ųą┐╝ŠW(w©Żng)Ż¼2025ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąąŻĪ>>³c(di©Żn)ō¶▓ķ┐┤